EL EJE INTESTINO-CEREBRO
Estela Fuentes • 28 de junio de 2023
En los últimos años se ha descubierto cada vez más evidencia sobre la comunicación bidireccional entre la microbiota del tracto digestivo y el sistema nervioso central, lo que se conoce como el eje intestino-cerebro. Este eje es un sistema de comunicación complejo que implica varias vías.
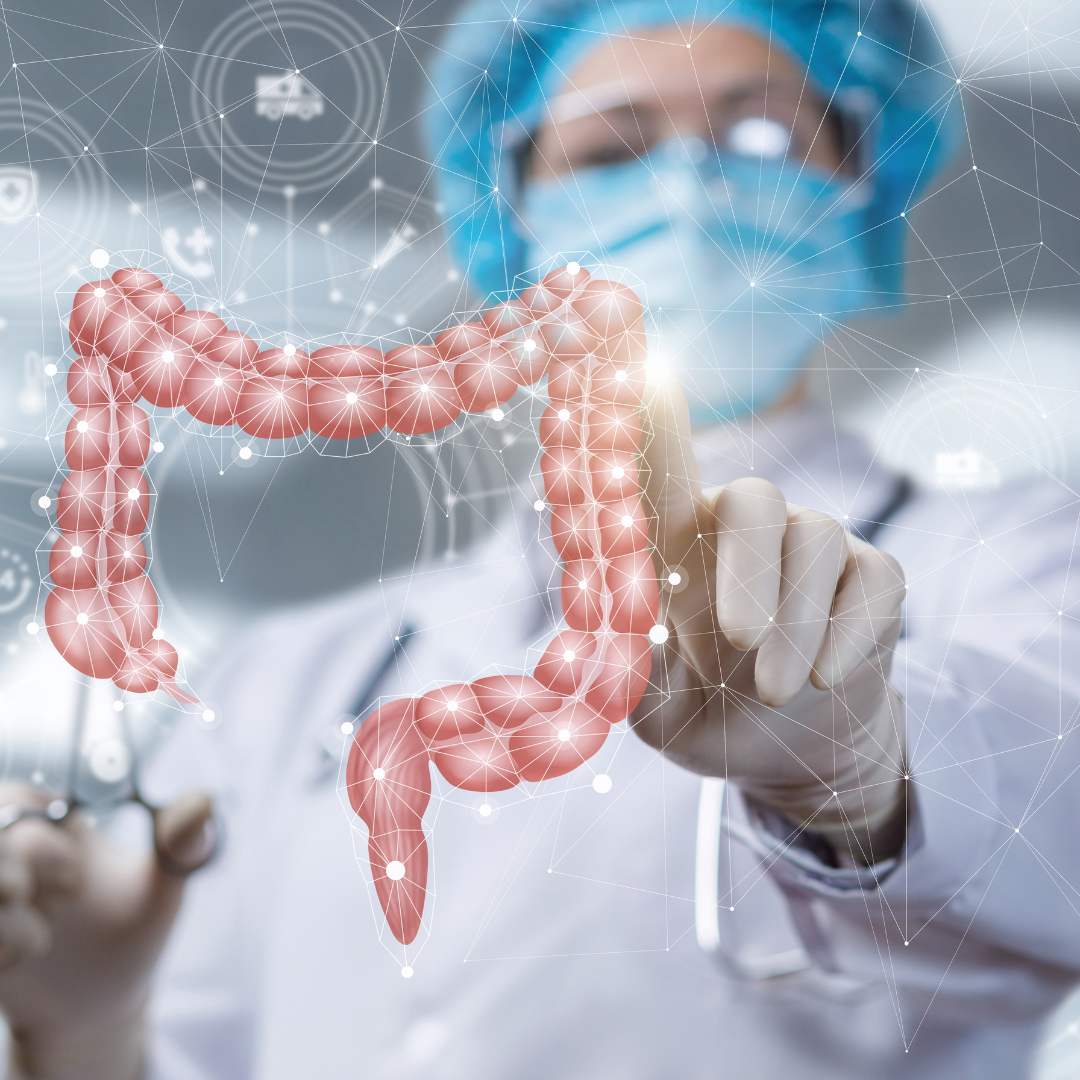
La primera vía es a través del nervio vago, que es el décimo par craneal y tiene una conexión directa entre el cerebro y el tracto gastrointestinal. A través del nervio vago, las señales pueden transmitirse en ambas direcciones, lo que permite una comunicación rápida entre el intestino y el cerebro.
La segunda vía es la vía sistémica, que implica la liberación de hormonas, metabolitos y neurotransmisores producidos por la microbiota intestinal. Estas moléculas pueden ingresar a la circulación sanguínea y llegar al cerebro, donde pueden influir en la función cerebral y el estado de ánimo.
La tercera vía es el sistema inmune, específicamente a través de la acción de las citocinas, que son proteínas liberadas por células del sistema inmunitario en respuesta a la presencia de microorganismos o inflamación. Estas citocinas pueden afectar la función cerebral y el comportamiento a través de su acción en el sistema nervioso central.
La interacción entre la microbiota intestinal y el cerebro es un área activa de investigación y se ha sugerido que desequilibrios en esta comunicación pueden estar relacionados con diversos trastornos neuropsiquiátricos, como la depresión, la ansiedad y el autismo. Comprender mejor el eje intestino-cerebro puede tener implicaciones importantes para el desarrollo de nuevas estrategias terapéuticas en el campo de la salud mental y gastrointestinal.
Efectivamente, el eje intestino-cerebro está compuesto por varios elementos interconectados, incluyendo la microbiota, el sistema nervioso entérico, el sistema nervioso autónomo, el sistema neuroendocrino, el sistema neuroinmune y el sistema nervioso central.
El sistema nervioso entérico es una red compleja de neuronas que se encuentra en la pared del tracto gastrointestinal y es responsable de regular las funciones básicas del sistema digestivo, como la motilidad y la secreción de mucosa. Por otro lado, el nervio vago establece una conexión directa entre el cerebro y el intestino, permitiendo una comunicación bidireccional entre ambos.
El sistema neuroendocrino también desempeña un papel importante en este eje, ya que las células neuroendocrinas presentes en el intestino pueden liberar hormonas y neurotransmisores que afectan tanto al sistema nervioso como al sistema inmunológico. Además, el sistema nervioso autónomo, que controla las funciones involuntarias del cuerpo, incluyendo las del tracto gastrointestinal, también está implicado en la comunicación entre el intestino y el cerebro.
El sistema neuroinmune, que involucra la interacción entre el sistema nervioso y el sistema inmunológico, también desempeña un papel relevante en este eje. Las células del sistema inmunológico presentes en el intestino pueden liberar citocinas y otros mediadores que pueden afectar la función cerebral.
Las alteraciones en la composición de la microbiota, conocidas como disbiosis, se han relacionado con diversas enfermedades y trastornos, incluyendo la encefalopatía hepática, la ansiedad, el autismo y el síndrome del intestino irritable. Estas alteraciones en la microbiota pueden afectar la motilidad gastrointestinal, las secreciones y la sensibilidad visceral, y a su vez, influir en la función de las células neuroendocrinas y del sistema inmunológico, lo que puede tener implicaciones en la manifestación de síntomas psiquiátricos.
Además, estudios en modelos animales han demostrado que diferentes situaciones de estrés pueden alterar la composición de la microbiota, lo que sugiere una comunicación bidireccional en este eje. Es decir, la microbiota puede influir en el comportamiento humano, y a su vez, las alteraciones en el eje intestino-cerebro pueden afectar la composición de la microbiota.
En resumen, el eje intestino-cerebro es un sistema complejo de comunicación bidireccional que involucra la microbiota, el sistema nervioso entérico, el sistema nervioso autónomo, el sistema neuroendocrino, el sistema neuroinmune y el sistema nervioso central. Las alteraciones en este eje se han asociado con diversas enfermedades y trastornos, y comprender mejor su funcionamiento puede tener implicaciones importantes para el diagnóstico y tratamiento de enfermedades tanto gastrointestinales como psiquiátricas.
Estela Fuentes PNIE
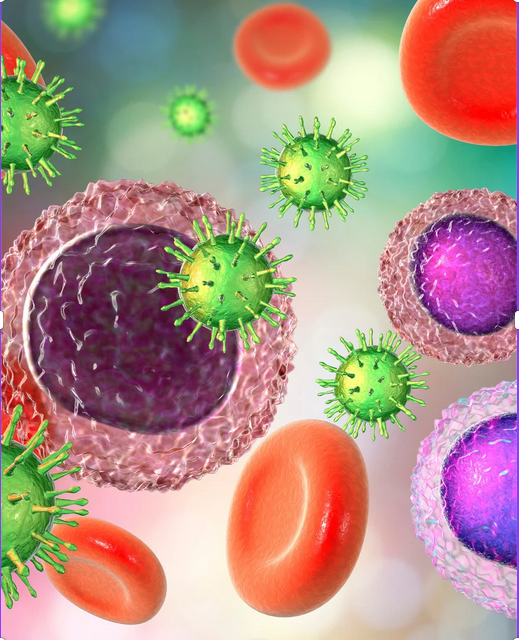
Las enfermedades autoinmunes son condiciones complejas y multifactoriales en las que el sistema inmunológico pierde su capacidad de distinguir entre lo propio y lo extraño, atacando tejidos y órganos del propio cuerpo. Desde la medicina convencional, el abordaje suele centrarse en frenar la respuesta inmunitaria, sin profundizar en las causas subyacentes. Sin embargo, desde la Psiconeuroinmunoendocrinología (PNIE), se propone un enfoque más holístico y causal, integrando los ejes clave que conectan el sistema nervioso, el sistema endocrino, el sistema inmunológico y el entorno psicoemocional del paciente. Microbiota intestinal: el epicentro de la inmunorregulación Numerosas investigaciones, han demostrado que la microbiota intestinal juega un papel determinante en el desarrollo y mantenimiento de la inmunotolerancia. Cuando esta microbiota se encuentra en disbiosis, la barrera intestinal se vuelve permeable, permitiendo el paso de moléculas inmunogénicas al torrente sanguíneo que activan respuestas inflamatorias y autoinmunes. Un intestino inflamado es un sistema inmune alterado. Además, la ruptura de la homeostasis entre microbiota, sistema inmune y barrera intestinal puede estar influenciada por factores como: Dietas proinflamatorias y ultraprocesadas Uso prolongado de antibióticos y medicamentos Estrés crónico Infecciones virales persistentes (como Epstein-Barr, EBV) Tóxicos ambientales y alteraciones hormonales El enfoque PNIE: más allá del síntoma La PNIE no trata enfermedades, sino personas. El objetivo es comprender qué ha roto el equilibrio interno y qué herramientas pueden restaurarlo. Este modelo integrativo contempla: 1. Abordaje nutricional personalizado Restaurar la microbiota con prebióticos, probióticos y simbióticos específicos Dietas antiinflamatorias y moduladoras del sistema inmune Revisión de intolerancias alimentarias, gluten, caseína, etc. 2. Gestión del estrés y regulación emocional El estrés psicoemocional sostenido activa el eje HPA (hipotálamo-hipófisis-adrenal), generando una sobreproducción de cortisol que altera la función inmune y promueve procesos inflamatorios. 3. Intervención sobre el contexto viral y tóxico Muchos casos de enfermedades autoinmunes se correlacionan con infecciones virales persistentes o exposición a metales pesados. Desde la PNIE se trabaja en la reducción de la carga tóxica y en la estimulación de las vías naturales de detoxificación. 4. Reequilibrio hormonal Particularmente en mujeres, el desequilibrio entre estrógenos y progesterona puede agravar procesos autoinmunes. Por eso es clave considerar el entorno endocrino del paciente. ¿Es posible revertir una enfermedad autoinmune? Aunque la medicina tradicional suele considerar las enfermedades autoinmunes como incurables, la experiencia clínica desde la PNIE sugiere que la remisión es posible en muchos casos cuando se aborda el terreno biológico y emocional de forma integrativa. El paciente deja de ser un simple receptor pasivo de tratamientos y se convierte en el protagonista activo de su salud. ¿Tienes una enfermedad autoinmune o conoces a alguien que la sufra? Tal vez ha llegado el momento de mirar más allá del diagnóstico y empezar un camino hacia el equilibrio. La salud no es la ausencia de síntomas, sino el resultado del equilibrio entre cuerpo, mente y entorno.

Enfermedades autoinmunes y epigenética: ¿El destino está escrito o lo escribimos nosotros? Hasta hace no mucho tiempo, el paradigma reinante nos llevaba a creer que nuestros genes eran como un destino inamovible, dictando nuestra salud y predisposición a enfermedades de manera inalterable. Sin embargo, los avances científicos han desafiado esta concepción estática y nos han revelado un mundo mucho más complejo y fascinante: la epigenética. La epigenética nos enseña que no todo está determinado por los genes que heredamos de nuestros ancestros. Si bien estos genes proporcionan el "potencial" para ciertas enfermedades o características, su expresión no está grabada en piedra. De hecho, nuestro estilo de vida y el ambiente que nos rodea juegan un papel crucial en decidir si esos genes se activarán o permanecerán silenciados. Imagina los genes como pistolas cargadas: tienen el potencial de causar daño, pero necesitan un gatillo para disparar. Aquí es donde entra en juego la epigenética. Este campo de estudio se encarga de estudiar las modificaciones químicas que ocurren en el ADN y en las proteínas asociadas, influenciando la actividad génica sin cambiar la secuencia de ADN en sí. En pocas palabras, la epigenética aprieta o suelta el gatillo de nuestros genes. Esto significa que las enfermedades que heredamos no son un destino inevitable. Inicialmente, estos genes pueden estar "desactivados", pero dependiendo de la interacción entre nuestro estilo de vida y el ambiente, pueden ser activados o permanecer en silencio. Por ejemplo, la dieta, el ejercicio, el estrés y la exposición a toxinas ambientales pueden influir en cómo se expresan nuestros genes y, por lo tanto, en nuestra salud. Esta comprensión más amplia nos empodera. Ya no somos simplemente marionetas de nuestros genes, sino que somos cocreadores de nuestra salud. Podemos tomar decisiones conscientes sobre nuestro estilo de vida y entorno, sabiendo que estas elecciones tienen un impacto directo en la activación o desactivación de nuestros genes. En resumen, la epigenética nos muestra que nuestro destino no está predeterminado por nuestros genes. Los genes pueden cargar la pistola, pero es la epigenética la que decide si se aprieta o no el gatillo. Este conocimiento nos invita a reflexionar sobre cómo podemos influir activamente en nuestra salud y bienestar, asumiendo un papel activo en la escritura de nuestro propio destino genético. .
